Articolo di Gian Carlo Ruggeri – Autore Ospite de La Lampadina
Dal 20 maggio di questo anno avrà inizio, in tutto il mondo, una rivoluzione silenziosa, di cui il normale cittadino non avrà contezza. Si tratterà di un transito basilare sotto l’aspetto culturale, economico e per la ricerca scientifica. Alla data succitata, infatti, saranno definite di nuovo tutte le unità di misura: i loro riferimenti non saranno più costituiti da modelli – campione, ma dalle costanti universali della fisica. Queste sono dei numeri che non cambiano, come, ad esempio, la velocità della luce, la carica di un elettrone e la costante di Planck (h).
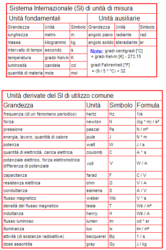 Facciamo un salto indietro: nel 1960, la comunità scientifica ha dato vita ad un Sistema Internazionale, denominato SI (Standard International) usato quasi in tutto il mondo. Questo Sistema è basato su sette unità fondamentali: il chikogrammo, il metro, il secondo, l’ampere, il kelvin, la mole e la candela. Non molto tempo dopo il 20 maggio 1875, data alla quale diciassette Paesi firmarono la Convenzione del Metro e, quindi, nacque la Metrologia moderna, il metro, inizialmente definito come “1/10 milionesimo del quarto del meridiano terrestre, compreso tra il Polo nord e l’Equatore, che passa per il meridiano di Parigi”, nel 1889, nella Prima Conferenza internazionale di pesi e misure, si decide di usare riferimenti solidi e, quindi, si creano dei campioni materiali del metro e del chilogrammo: il primo costituito dalla Barra n. 27 di platino – iridio conservata alla temperatura costante di 0°C, il secondo (Grand – Kilo) da un cilindro di altezza e diametro pari a 0,039 m, in lega di platino – iridio.
Facciamo un salto indietro: nel 1960, la comunità scientifica ha dato vita ad un Sistema Internazionale, denominato SI (Standard International) usato quasi in tutto il mondo. Questo Sistema è basato su sette unità fondamentali: il chikogrammo, il metro, il secondo, l’ampere, il kelvin, la mole e la candela. Non molto tempo dopo il 20 maggio 1875, data alla quale diciassette Paesi firmarono la Convenzione del Metro e, quindi, nacque la Metrologia moderna, il metro, inizialmente definito come “1/10 milionesimo del quarto del meridiano terrestre, compreso tra il Polo nord e l’Equatore, che passa per il meridiano di Parigi”, nel 1889, nella Prima Conferenza internazionale di pesi e misure, si decide di usare riferimenti solidi e, quindi, si creano dei campioni materiali del metro e del chilogrammo: il primo costituito dalla Barra n. 27 di platino – iridio conservata alla temperatura costante di 0°C, il secondo (Grand – Kilo) da un cilindro di altezza e diametro pari a 0,039 m, in lega di platino – iridio.
 Ma i campioni materiali si alterano nel corso del tempo: il metro diminuisce in lunghezza e il chilogrammo, seppur conservato sotto tre campane di vetro ed in cassaforte, ha subito un calo ponderale di 50 microgrammi durante la propria esistenza. È evidente che se questa differenza potrebbe essere troppo piccola e priva di importanza costruendo degli hamburger, ai fini delle misurazioni scientifiche, che devono possedere un elevatissimo grado di precisione, la definizione del chilogrammo può causare seri problemi. Per questo, la definizione del metro, nel corso degli anni, è cambiata due volte ancora: la prima volta nel 1960, ancorando la definizione stessa ad una transizione dell’isotopo 86 del Kripton e la seconda nel 1983, allorché, nella XVII Conferenza Generale di pesi e misure essa diviene “La distanza percorsa dalla luce nel vuoto in 1/299 792 458 di secondo”.
Ma i campioni materiali si alterano nel corso del tempo: il metro diminuisce in lunghezza e il chilogrammo, seppur conservato sotto tre campane di vetro ed in cassaforte, ha subito un calo ponderale di 50 microgrammi durante la propria esistenza. È evidente che se questa differenza potrebbe essere troppo piccola e priva di importanza costruendo degli hamburger, ai fini delle misurazioni scientifiche, che devono possedere un elevatissimo grado di precisione, la definizione del chilogrammo può causare seri problemi. Per questo, la definizione del metro, nel corso degli anni, è cambiata due volte ancora: la prima volta nel 1960, ancorando la definizione stessa ad una transizione dell’isotopo 86 del Kripton e la seconda nel 1983, allorché, nella XVII Conferenza Generale di pesi e misure essa diviene “La distanza percorsa dalla luce nel vuoto in 1/299 792 458 di secondo”.
Il tempo passa, però, e le unità fondamentali di misura da tre (metro, 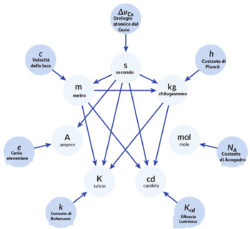 chilogrammo, secondo), sono diventate sette (in più vi sono l’ampere, le unità di misura della temperatura, la mole e la candela – fra queste ultime due, la prima serve per misurare la quantità di sostanza e la seconda per l’intensità luminosa).
chilogrammo, secondo), sono diventate sette (in più vi sono l’ampere, le unità di misura della temperatura, la mole e la candela – fra queste ultime due, la prima serve per misurare la quantità di sostanza e la seconda per l’intensità luminosa).
Nel frattempo, il “secondo”, definito come “1/86400 del giorno solare medio”, ha subito un accorciamento a causa dell’allungamento delle giornate causato dall’interazione gravitazionale Terra – Luna e dalle forze di marea, e, pertanto, nel 1967 viene adottato il secondo del Tempo atomico internazionale (la durata di 9 192 631 770 periodi della radiazione corrispondente alla transizione tra due livelli iperfini dello stato fondamentale dell’atomo di Cesio – 133) e, quasi contemporaneamente, anche la candela ha subito due definizioni correlate a due costanti. A conti fatti, pertanto, restando da ridefinire il chilogrammo, l’ampere, il kelvin e la mole, la 26^ Conferenza generale di pesi e misure (Versailles, 13/16 novembre 2018) ha adottato il nuovo Sistema SI, che – appunto – andrà in vigore il prossimo 20 maggio 2019, data in cui, come su accennato, oltre alle tre unità di base definite secondo costanti della fisica, oggi in vigore: il secondo (dal 1967), la candela ( (dal 1979) e il metro (dal 1983), verranno aggiunte il chilogrammo (secondo la costante di Planck), l’ampere (A, in termini di carica elementare), il grado Kelvin (K, costante di Boltzmann)e l’ampere (A, costante di Avogadro: numero di atomi presenti in 12 grammi di carbonio 12).
